安全性情報適正使用ガイドより抜粋
注意を要する副作用とその対策
頻脈性不整脈(QT延長を含む上室性及び心室性不整脈)
- QT間隔の延長があらわれるおそれがあります。
- 本剤の投与開始前及び投与中に心電図を測定することが望ましいです。
- QT延長を起こすことが知られている薬剤(アミオダロン、モキシフロキサシン、キニジン等)との併用には十分に注意してください。
発現状況
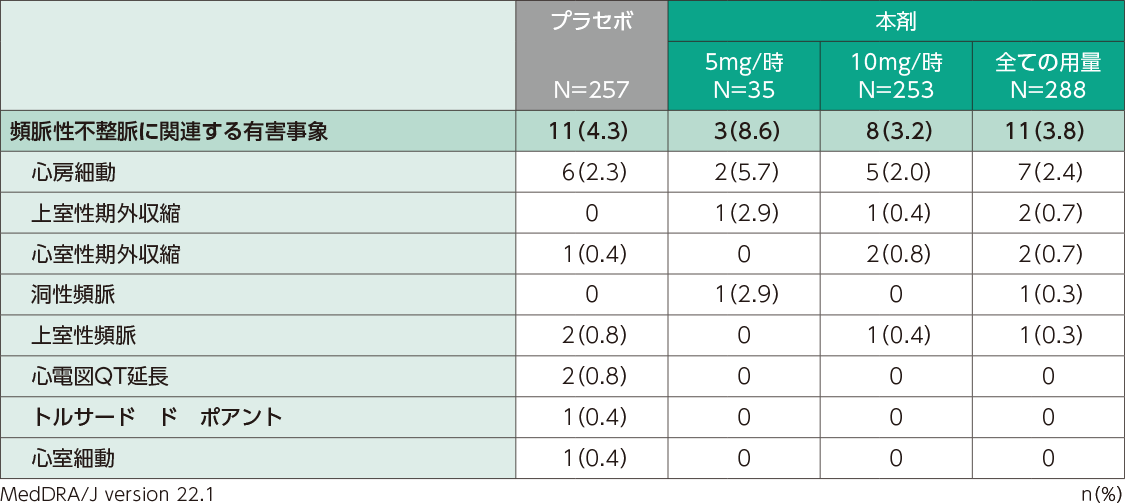
国内第Ⅱ相及び第Ⅲ相臨床試験での頻脈性不整脈関連の有害事象の発現割合は、本剤投与群で3.8%(11/288例)、プラセボ群で4.3%(11/257例)であり、プラセボ群の1例にトルサード ド ポアントが認められました。
頻脈性不整脈に関連する有害事象(日本人安全性解析対象集団)
健康成人35例を対象とした海外臨床試験において、本剤を高用量(20mg/時及び60mg/時を各3時間)静脈内持続投与し、QT間隔に及ぼす影響を検討した結果、QT間隔の延長が認められました。
対処法
心電図異常が認められた場合には、本剤の投与を中止するなど適切な処置を行ってください。
- 6. 用法及び用量
- 通常成人には、クラゾセンタンとして300mg(12mL)を生理食塩液500mLに加え、容量型の持続注入ポンプを用いて、17mL/時の速度で静脈内に持続投与する(クラゾセンタンとして10mg/時)。くも膜下出血術後早期に本剤の投与を開始し、くも膜下出血発症15日目まで投与する。なお、肝機能、併用薬に応じて適宜減量する。

