製品情報
作用機序
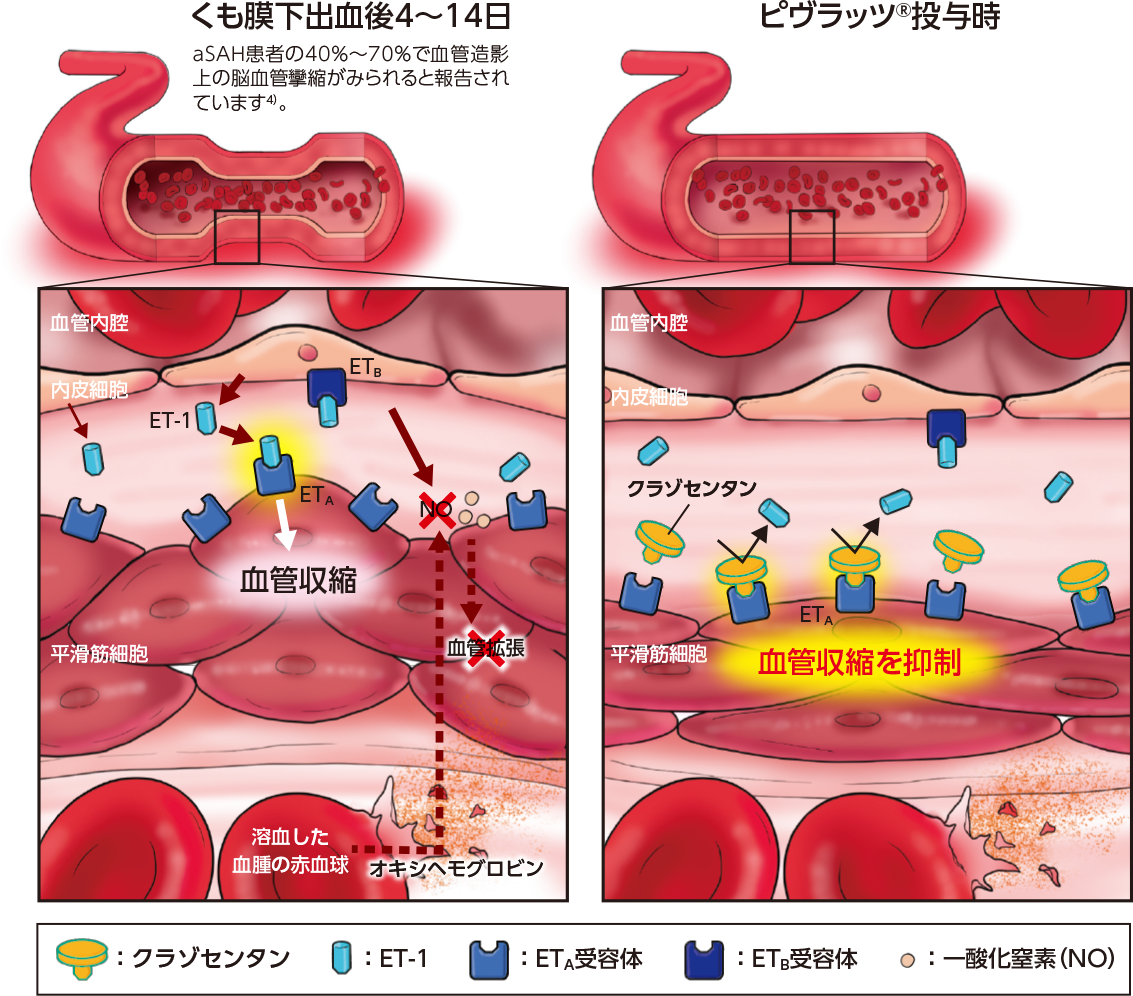
エンドセリン(ET)は、主に内皮細胞から産生される21のアミノ酸残基からなるペプチドで、ET-1、ET-2、ET-3の三つのアイソフォームが知られています1)。ET-1は、強力な血管収縮物質で、その受容体にはA型(ETA)受容体とB型(ETB)受容体があり、それらに結合するとGタンパク質をはじめとする細胞内シグナル伝達分子を活性化して細胞応答を引き起こします。
ETA受容体は、主に血管平滑筋細胞膜上に発現しており、ET-1が結合するとジアシルグリセロール及びイノシトール1,4,5-三リン酸(1,4,5-IP3)が産生され、これが直接又はプロテインキナーゼCを介して血管平滑筋細胞の細胞内カルシウム濃度を上昇させることにより、血管の収縮を誘発します2)。
一方、ETB受容体は、主に血管内皮細胞膜上に発現しており、ET-1が結合すると一酸化窒素(NO)の産生を促して血管拡張を誘発します。しかし、くも膜下出血後では溶血した赤血球由来のオキシヘモグロビンがNOと結合するため、この作用は阻害されます。
このようにET-1は、脳動脈瘤によるくも膜下出血患者の脳血管攣縮の病態生理に関与しています。
ピヴラッツ®は、ETA受容体に対して選択的な拮抗作用を示し、血管収縮を抑制し、脳血管攣縮を抑えます。 ETB受容体に比べ、ETA受容体に対して最大で約1,000倍の結合親和性を示し、125I-ET-1結合に対するKi値は0.13~1.7nmol/Lでした3)。
血管収縮に対する作用
(1)ETA及びETB受容体へのET-1結合に対する作用(in vitro)1,2)
ヒトETA及びETB受容体の相補的DNA(cDNA)を安定的に過剰発現させたチャイニーズハムスター卵巣(CHO)細胞、アフリカミドリザル腎(COS)細胞、バキュロウイルス感染昆虫(Sf9)細胞から単離したミクロソーム膜のほか、ヒト胎盤、ラット内皮細胞並びにラット及びブタの気管から採取した細胞膜に対する放射性ヨウ素標識(125I-)ヒトET-1、ET-3及びサラフォトキシン(SRTX)S6cの結合アッセイを実施しました。
クラゾセンタンはこれらの細胞及び組織のETA受容体への125I-ET-1の特異的結合を強力に阻害し、阻害定数(Ki値)は0.13~1.7nmol/Lでした。ETB受容体リガンドである125I-ET-1、125I-ET-3又は125I-SRTX S6cのETB受容体への特異的結合に対するクラゾセンタンの阻害作用は弱く、クラゾセンタンはETA受容体に対して最大で約1,000倍の選択性を示すと考えられました。各受容体サブタイプに対応するHill係数はいずれも1に近かったことから、競合的阻害と考えられました。
in vitroにおけるエンドセリン受容体に対するクラゾセンタンの結合活性
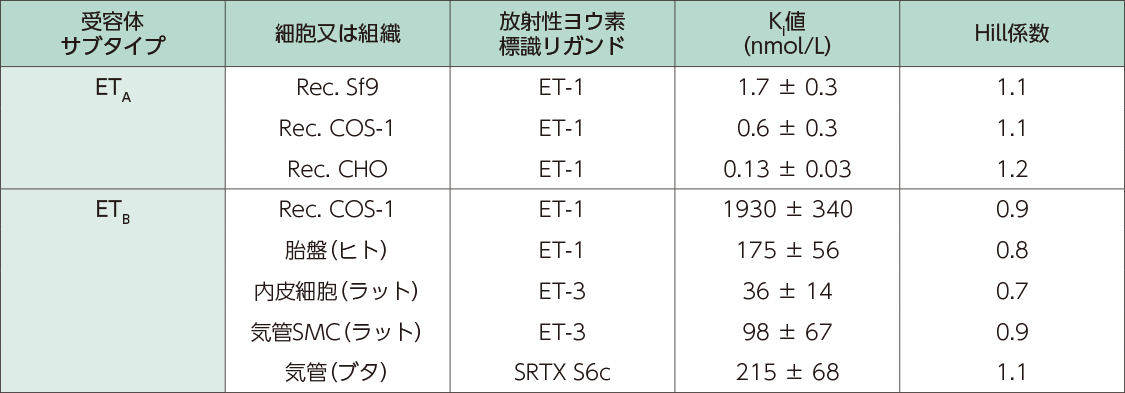
CHO:チャイニーズハムスター卵巣細胞、SMC:平滑筋細胞、SRTX:サラフォトキシン、Ki 値:阻害定数(平均値±標準誤差)、
Hill 係数:酵素反応の協同性を示す指標
1)Roux S, et al.: J Pharmacol Exp Ther. 1997; 283(3): 1110-1118.
2)社内資料:薬効薬理試験in vitro
(2)ET-1を介したイノシトール三リン酸及びカルシウムシグナル伝達に対する作用(in vitro)1,2)
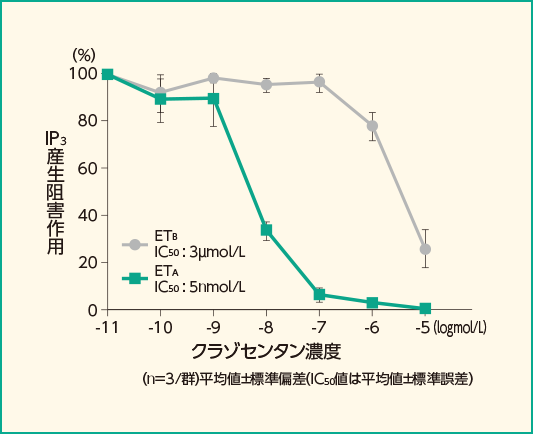
ヒトETA又はETB受容体を強制発現させたCOS-1細胞を用いて、クラゾセンタンによるETA及びETB受容体の機能阻害作用を評価した結果、クラゾセンタンはET-1を介したイノシトール1,4,5-三リン酸(IP3)の産生を阻害し、その50%阻害濃度(IC50値)はETA受容体に対して5nmol/L、ETB受容体に対して3μmol/Lであり、ETB受容体と比較してETA受容体に約600倍の選択性を示しました。
クラゾセンタンのETA受容体への高い選択性は、ETA又はETB受容体を一過性に発現させたヒト胎児腎(HEK)
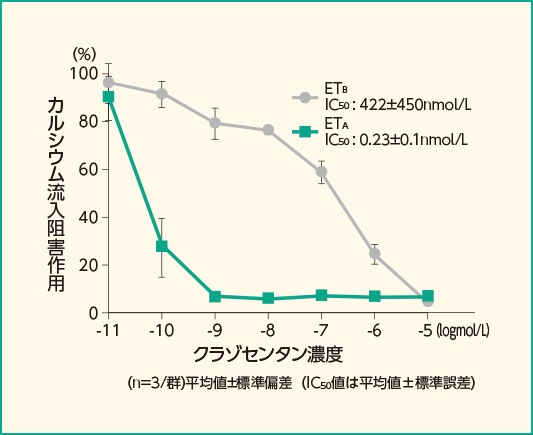
293細胞におけるET-1誘発細胞内カルシウム流入に対する阻害作用からも確認されました。クラゾセンタンはカルシウム流入を濃度依存的に阻害し、IC50値(平均値±標準誤差)はETA受容体に対して0.23±0.1nmol/L、
ETB受容体に対して422±450nmol/Lでした。422±450nmol/Lでした。
ET-1を介したIP3産生に対する作用(COS-1細胞)
ET-1を介した細胞内カルシウム流入に対する作用(HEK293細胞)
1)Roux S, et al.: J Pharmacol Exp Ther. 1997; 283(3): 1110-1118.
2)社内資料:薬効薬理試験in vitro
(3)摘出組織におけるET-1誘発収縮に対する作用(in vitro)1,2)
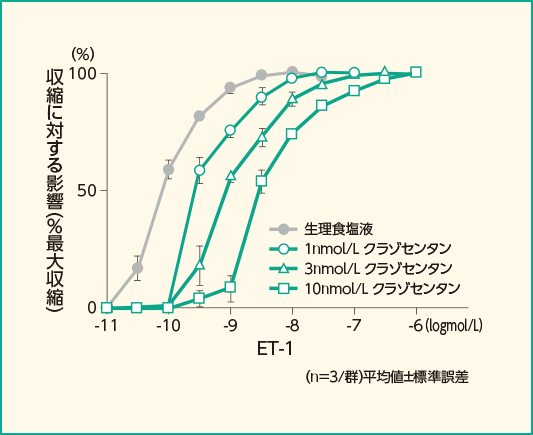
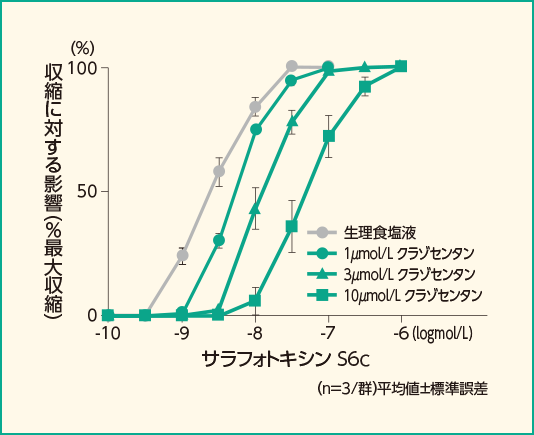
クラゾセンタンはラットから摘出した内皮剥離大動脈のET-1誘発収縮(ETA受容体介在性)及び上皮剥離気管のサラフォトキシンS6c刺激誘発収縮(ETB受容体介在性)を阻害し、そのpA2値はそれぞれ9.5及び6.4であり、 ETB受容体と比較してETA受容体に対して約1,000倍の選択性を示しました。
ET-1(10-11~10-6mol/L)誘発収縮に対するクラゾセンタンの影響
サラフォトキシンS6c(10-10~10-6mol/L)誘発収縮に対するクラゾセンタンの影響
1)Roux S, et al.: J Pharmacol Exp Ther. 1997; 283(3): 1110-1118.
2)社内資料:薬効薬理試験in vitro
(4)脳血管攣縮に対する作用(イヌ及びウサギ)3)
クラゾセンタンはイヌ及びウサギのくも膜下出血モデルにおいて脳血管攣縮を抑制しました。
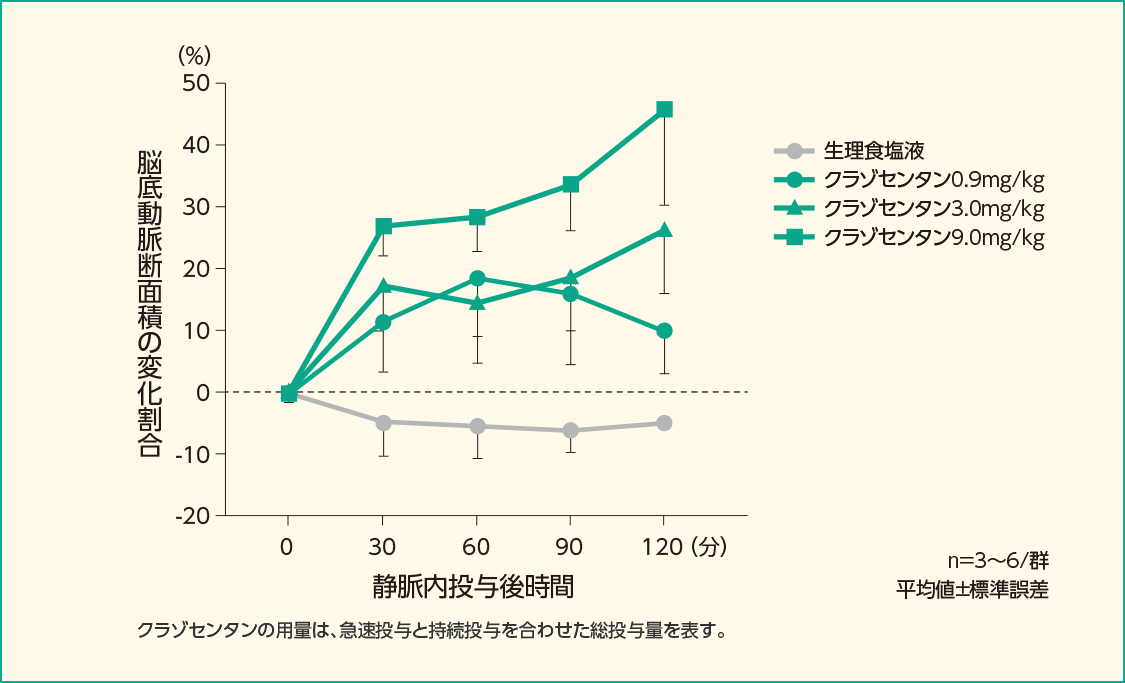
- イヌの大槽に自家血を2日連続で注入することによりSAHに関連する脳血管攣縮を誘発し、麻酔下で媒体(生理食塩液)又はクラゾセンタン(0.3、1、3mg/kg)を静脈内急速投与後、1時間あたりの用量が急速投与時と同じになるように2時間の静脈内投与を行いました(総投与量は0.9、3、9mg/kg)。その結果、クラゾセンタンを静脈内急速投与後30分において、脳底動脈は用量依存的に拡張しました。2時間の持続投与後には、9mg/kgのクラゾセンタンにより脳底動脈断面積が投与前と比較して47±16%増加しました。
クラゾセンタンを静脈内投与した時の脳底動脈断面積の変化(イヌ)
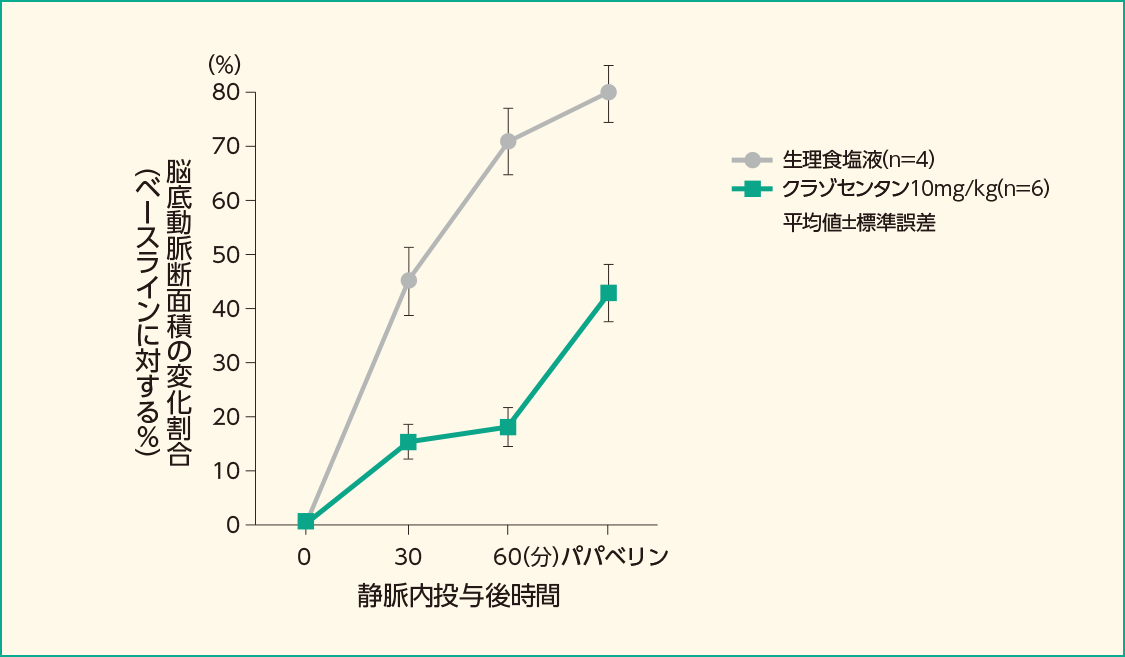
- ウサギの大槽に自家血を注入することによりSAHに関連する脳血管攣縮を誘発し、48時間後に媒体(生理食塩液)又はクラゾセンタン10mg/kgを静脈内急速投与し、脳底動脈の血管造影を投与前、投与後30及び60分後に実施後、パパベリンを椎骨動脈内に投与して脳底動脈を最大限に拡張させ脳底動脈の血管造影を実施しました。クラゾセンタンにより脳底動脈断面積はパパベリンによる最大反応の89%まで増加しました(媒体群:42%増加)。
クラゾセンタンを静脈内投与した時の脳底動脈断面積の変化(ウサギ)