安全性情報適正使用ガイドより抜粋
注意を要する副作用とその対策
体液貯留(胸水、肺水腫、脳浮腫)
本剤の投与により体液貯留(胸水、肺水腫、脳浮腫)が発現することがあります。
- 11. 副作用 11.1 重大な副作用
- 11.1.1 体液貯留:胸水(13.3%)、肺水腫(11.0%)、脳浮腫(0.5%)
発現状況
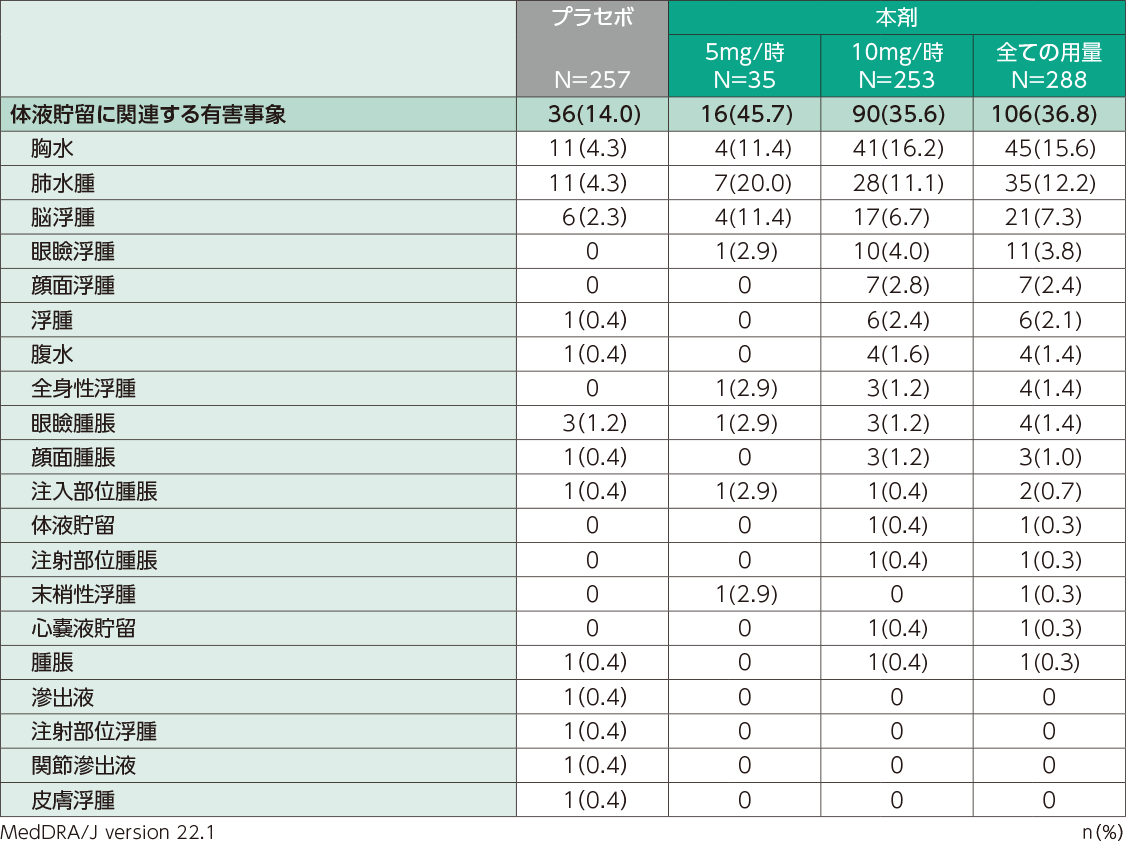
国内第Ⅱ相及び第Ⅲ相臨床試験での体液貯留関連の有害事象の発現割合は、本剤投与群で36.8%(106/288例)、プラセボ群で14.0%(36/257例)でした。主な体液貯留関連の有害事象は、胸水[本剤投与群15.6%(45/288例)、プラセボ群4.3%(11/257例)]、肺水腫[本剤投与群12.2%(35/288例)、プラセボ群4.3%(11/257例)]、及び脳浮腫[本剤投与群7.3%(21/288例)、プラセボ群2.3%(6/257例)]でした。
体液貯留に関連する有害事象(日本人安全性解析対象集団)
初期症状
喀痰、咳嗽、息切れ、頻拍、頭痛、眩暈、視力低下等
対処法
本剤投与中は体液量の調節に留意し、体液貯留の初期症状を十分に観察してください。特に、Triple H療法又はHyperdynamic療法が併用される場合は、体液貯留リスクが増強するおそれがあるため、慎重に体液量を管理してください。

